Patrice Debré
Professeur émérite d’immunologie à Sorbonne Université, membre de l’Académie nationale de médecine
Les microbes sont responsables de 25% des décès (14 millions de morts), dont les deux tiers sont des enfants, atteignant principalement les pays à ressources limitées. En même temps, ils vivent en nous, avec nous, pour nous, en germes commensaux de l’homme : c’est le microbiote.
Le terme microbiote désigne l’ensemble des microbes qui habitent l’homme et cohabitent avec lui, quelle que soit leur localisation anatomique, sur la peau, dans le conduit auditif, les bronches, la cavité vaginale, etc. [1, 2]. Les recherches sur le microbiote ont cependant essentiellement porté sur les bactéries et leur présence dans le tube digestif, où l’on en trouve le plus grand nombre, mais aussi parce c’est là que leur influence sur la physiologie de l’organisme semble déterminante.
Il y a 100 milliards de bactéries dans un gramme de selles, autant que de cellules qui constituent notre cerveau, même si les neurones sont de plus grande taille. Entre la bouche et l’anus, sur une surface considérable de près de 400 m2, plusieurs centaines de milliards de bactéries cohabitent, sans compter les virus et les champignons. Les microbes qui habitent l’homme ont ainsi fait la conquête d’un autre environnement. Les effets heureux de la sélection naturelle ont sans doute aussi apporté leur contribution à l’humanité en passant du parasitisme agressif à la symbiose. Hommes, animaux ou plantes abritent, depuis leur apparition sur terre, des virus, bactéries ou champignons qui leur préexistaient et dont ils assurent, de manière asymétrique, l’habitat, la nourriture, parfois la défense. Au fur et à mesure de l’évolution, l’inverse s’est pourtant produit. L’hôte exige la réciprocité. On passe alors à un état de mutualisme ou de symbiose, forme sans doute la plus aboutie de la co-évolution.
Les territoires et fonctions du microbiote digestif
La bouche héberge plus de 320 espèces différentes de bactéries commensales, réparties entre la salive, les lèvres, les joues, le palais, la langue, les dents et la gencive. Plusieurs millions de germes sont présents par millilitre de salive. Des espèces peuvent encore y être découvertes. La plus célèbre des bactéries qui prolifèrent dans l’œsophage et l’estomac est Helicobacter pylori, seule capable de survivre en milieu aussi acide, mais aussi de donner des ulcères. Si l’on poursuit l’étude des bactéries du tube digestif, dans la dernière partie de l’intestin grêle, l’iléon, vit une population plus importante de microbes, de l’ordre de 100 millions de bactéries par gramme de matière, qui fait de ces dernières la part essentielle de ce qu’on peut y trouver. La flore y est cependant assez mal définie car son examen nécessite des prélèvements par chirurgie ou intubation, mais sa diversité est proche de celle observée dans les selles. Dans le côlon, la diversité et le nombre des bactéries sont considérables, mille fois supérieurs à leur concentration dans l’iléon. La moitié de la matière qui constitue les selles correspond à des bactéries. Seules subsistent les anaérobies strictes. Ainsi les bactéries Escherichia coli, qui se sont ainsi adaptées à la vie sans oxygène, y prolifèrent.
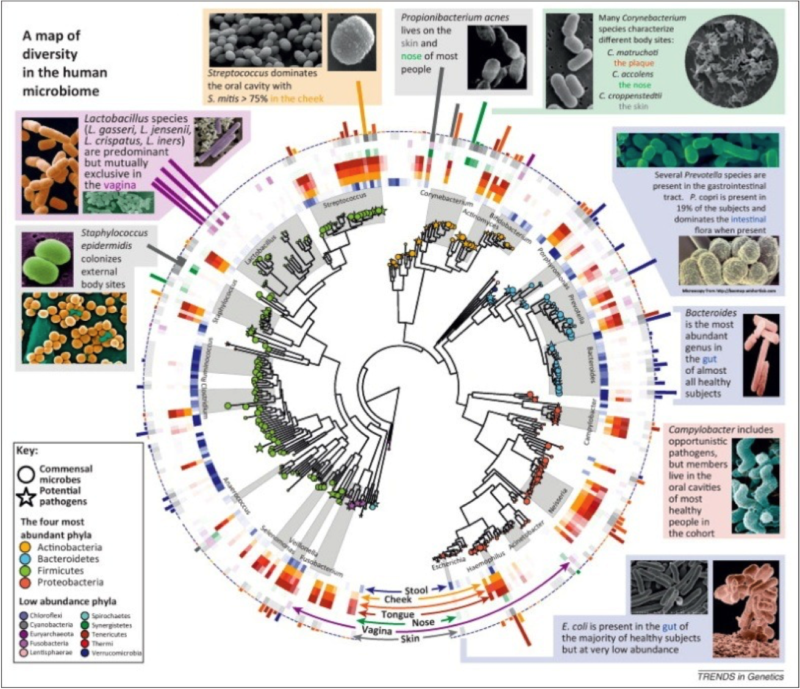
Le microbiote est unique à chacun de nous, même s’il comporte une grande diversité (cf. figure). Deux grands groupes bactériens dominent : les firmicutes et les bactéroïdes. Ces deux grandes populations correspondent à plus de 80% des bactéries de notre intestin. Pourtant elles divergent presque autant que les règnes animal et végétal. Les firmicutes représentent une espèce qui comprend des germes très courants et connus comme le staphylocoque ou le streptocoque. D’autres, comme le Lactobacillus bulgaris, sont moins connus. Les bactéroïdes représentent le groupe le plus important de bacille à Gram négatif. Ils sont essentiellement anaérobies. Si plus de 250 espèces ont ainsi été identifiées dans ces deux phylums majeurs, il existe de nombreuses autres bactéries dans la microflore. Elles appartiennent majoritairement à deux autres groupes, les Actinobacteria et les Proteobacteria, parmi lesquelles des bactéries réductrices de soufre. Mais on trouve aussi des archéobactéries.
Les deux tiers des espèces intestinales dominantes qu’héberge chaque individu adulte lui sont totalement spécifiques. Le tiers restant étant plus ou moins partagé selon les individus. Bien entendu, cet équilibre dépend de l’alimentation, de la prise d’antibiotiques, de l’hygiène. Chez un même individu, les grands équilibres entre espèces varient cependant peu, malgré les éventuelles modifications de régime alimentaire. La flore intestinale reste difficile à étudier. Il faut en effet la prélever. Aussi se réfère-t-on plus facilement au microbiote fécal que cæcal, malgré les différences entre les deux. Il y a quelques années, l’analyse ne pouvait être fondée que sur les techniques de culture qui, selon leur composition, permettaient une sélection par genre ou espèce, ou au contraire leur prolifération en masse. Aux critères de forme phénotypique et de caractérisation du métabolisme bactérien sont venues s’adjoindre aujourd’hui les données de la génomique qui ont permis l’analyse simultanée de l’ensemble des populations microbiennes, la métagénomique.
Né stérile – sa condition in utero –, le nouveau-né se trouve propulsé dans un univers microbien riche et varié, celui de sa mère. De manière étonnante cependant, malgré l’extraordinaire diversité des microbes maternels, il est colonisé de façon rapide et massive par un microbiote relativement simple qui va se modifier par l’allaitement. D’autres éléments influencent encore l’implantation et la composition de la flore intestinale : le mode d’accouchement, l’environnement, le type d’alimentation, l’âge à la naissance et l’antibiothérapie.
Le microbiote a deux grandes fonctions principales, capitales pour l’homme : il permet la digestion de l’amidon et des sucres complexes des fibres alimentaires ; il joue un rôle dans l’activation, la différenciation et l’homéostasie du système immunitaire, lui permettant de tolérer les microbes commensaux et d’éliminer les pathogènes.
Le microbiote permet la digestion de l’amidon et des sucres complexes des fibres alimentaires
Une part importante de l’amidon se déverse dans le côlon sans avoir été préalablement transformé. Cette portion, qu’on appelle amidon résistant, sert à la prolifération des bactéries qui transforment les aliments amidonnés et permettent leur absorption. Les fibres alimentaires se déversent dans le gros intestin où elles se trouvent confrontées à de très nombreuses enzymes bactériennes différentes, capables de détruire tous les sucres des grains, tubercules, rhizomes, fruits. Les bactéries ne s’attaquent cependant pas qu’aux sucres alimentaires, elles digèrent aussi le mucus. Sans bactéries, le mucus, qui est continuellement secrété et jusqu’à des quantités considérables, entraînerait une distension colique, comme cela est observé chez les souris axéniques ou chez les hommes qui vivent sans germes. La dégradation par le microbiote des protéines présentes dans le côlon génère de nombreuses substances métaboliques potentiellement toxiques pour l’hôte. Elles sont dégradées en peptides, qui sont la principale source azotée du gros intestin. Cette hydrolyse est indispensable aux bactéries dont la prolifération requiert des hydrates de carbone et des composés d’azote. Si la structure, la solubilité, le temps de transit jouent dans cette décomposition, l’essentiel provient d’enzymes bactériennes, les protéases, actives dans la partie distale du côlon où l’acidité est la plus forte. Les peptides par eux-mêmes ont un rôle important sur la biodiversité du microbiote colique. Outre la production d’acides gras correspondant à la fermentation des acides aminés, un des principaux corps produits par cette transformation est l’ammoniaque. Absorbée par la muqueuse colique, l’ammoniaque est transportée vers le foie où elle est transformée en urée, puis éliminée dans les urines. La production est cependant faible et sans effet notable sur la santé dans les régimes alimentaires équilibrés. Les lipides qui parviennent dans le côlon sont très divers. Le microbiote peut également les utiliser ou les transformer. Certaines bactéries agissent sur le cholestérol en le transformant en un corps qui ne peut être absorbé et qui est éliminé dans les selles, jouant ainsi un rôle dans la régulation de son métabolisme. Une part importante des sels biliaires produits à partir du cholestérol parviennent également jusqu’au côlon où ils sont métabolisés par les bactéries. Les bactéries du microbiote sont, de plus, une source importante de vitamines, parmi lesquelles les vitamines K, B12 mais aussi B1, B2, B6 et B9.
Les microbes commensaux ont une action majeure sur l’activation et la différenciation lymphoïdes
Ils induisent un faible niveau d’activation du système immunitaire par une inflammation physiologique autorisant leur tolérance, tandis qu’un pathogène conduit à une réaction d’une autre ampleur. Les microorganismes établissent une continuité entre ces deux extrêmes : commensaux et pathogènes se différencient par leur capacité à moduler la réponse immunitaire de l’hôte. Mieux encore, les bactéries résidentes éduquent le système immunitaire, l’entraînent à lutter contre les germes délétères. La plupart des connaissances sur ce sujet proviennent des études comparatives entre les animaux axéniques dépourvus de microbiote et leurs congénères élevés dans les conditions classiques des animaleries de laboratoire. Les rongeurs maintenus en milieu stérile présentent une raréfaction des structures lymphoïdes enchâssées dans la muqueuse de la partie terminale de l’intestin grêle, les plaques de Peyer. La réponse immunitaire intestinale mobilise ces formations de lymphocytes B et T. Leur développement anormal s’accompagne d’un déficit de l’épithélium digestif en lymphocytes. La rate et les ganglions lymphatiques disséminés dans tout le corps présentent également des anomalies architecturales et des zones lymphocytaires atrophiées, immatures. L’absence de stimulation par les commensaux est donc à l’origine d’une atrophie des organes lymphatiques secondaires qui dépasse la sphère digestive, affecte l’ensemble des zones lymphoïdes et perturbe l’homéostasie immunitaire de l’organisme dans sa globalité, notamment du fait d’une carence en lymphocytes matures. En plus de leur quantité, le microbiote préserve l’équilibre qualitatif des cellules de l’immunité. Certaines populations bactériennes favorisent la production de lymphocytes T dits Th17, qui ont un rôle important dans l’organisation de la réponse immune protectrice, tandis que d’autres bactéries stimulent les lymphocytes T régulateurs qui inhibent cette réponse. Les commensaux participent ainsi à l’équilibre entre tolérance et rejet, ils maintiennent le système immunitaire entre action et inhibition. Le microbiote n’a donc pas qu’une mission locale de maintien de l’équilibre entre les cellules immunes de l’intestin et les bactéries qui y prolifèrent. Il joue un rôle plus important pour l’homéostasie du système immunitaire.
Les menaces du microbiote
Le microbiote est lié à une série de pathologies dont il peut représenter, au moins indirectement, des facteurs favorisants et ainsi de nouvelles cibles thérapeutiques.
Le microbiote tient aujourd’hui une bonne place parmi les éléments qui favorisent la surcharge pondérale. Car la flore intestinale est particulière chez les sujets obèses. Elle y est globalement moins diversifiée, avec une augmentation des firmicutes et une diminution des bactéroïdes. Si on examine attentivement le spectre des gènes microbiens par étude métagénomique, l’analyse du microbiote des patients obèses révèle certaines spécificités. Il se caractérise par une prévalence élevée de cinq populations de bactéries qui ne varient pas qu’en nombre. Ces bactéries ont des fonctions particulières capables d’induire diverses manifestations délétères pour l’organisme. La moindre diversité génétique des souches est associée à une résistance à l’insuline, qui peut conduire au diabète, à une anomalie des lipides et à un syndrome inflammatoire que signent une série de biomarqueurs dosés dans le sang. D’autres éléments rattachent le microbiote à l’obésité. Ainsi le transfert de flore intestinale de souris obèses à leurs congénères non obèses induit une prise de poids importante chez les souris nouvellement colonisées.
Le microbiote semble jouer également un rôle dans les cancers coliques. On constate en effet une modification importante des populations de bactéries dans les selles des patients cancéreux : augmentation des anaérobies, notamment du groupe des bactéroïdes, avec production de toxines inflammatoires et, parallèlement, diminution du nombre des firmicutes. Ces modifications ne se retrouvent pas que dans les selles, elles existent aussi au contact de la tumeur, où les germes anaérobies prolifèrent. Elles s’accompagnent d’une diminution de la production de butyrate, métabolite d’importance qui représente le principal substrat énergétique de l’épithélium intestinal et, de plus, a un effet trophique sur le biofilm bactérien. En supprimant le premier biofilm de bactéries commensales et protectrices, on laisse la place à des microorganismes qui, insuffisamment contrôlés par la réponse immunitaire, suscitent une multiplication désordonnée des cellules intestinales jusqu’à les rendre cancéreuses. Ce mécanisme, à la fois simple et complexe, peut être résumé et reproduit dans des modèles de souris. Il suffit d’introduire une modification du biotope pour induire des cassures chromosomiques dans les cellules intestinales et passer d’un stade purement inflammatoire, une altération bénigne, à la genèse du cancer.
Il est depuis longtemps admis qu’il existe un axe cerveau–intestin. Le cerveau influence les capacités motrices, sensitives et sécrétoires dans l’intestin. Nous devons au cerveau le péristaltisme intestinal qui assure la progression des aliments, mais aussi du microbiote, par la motilité qu’il instille à travers 200 millions de neurones, soit mille fois moins que le cerveau lui-même, mais autant que le cortex d’un chien ou d’un chat. 95% de la sérotonine, un des médiateurs du système nerveux qui participe à la gestion de nos émotions, est sécrétée par l’intestin. Les sécrétions bactériennes peuvent influencer le cerveau en produisant des neurotransmetteurs. Le nerf vague transmet directement les informations des viscères à l’hypothalamus, structure profonde du cerveau essentielle dans les comportements émotionnels, et à l’amygdale, une zone cérébrale qui coordonne des activités végétatives et sensitives. Tous ces éléments donnent ainsi du poids à une série d’expériences qui, depuis quelques années, relient le microbiote au comportement. Ainsi, des souris qui naissent par césarienne et ne possèdent pas les microbes qui vivent normalement dans le vagin ou le rectum maternel, semblent plus anxieuses que leurs congénères nées par voie basse. De meilleures preuves viennent de la transplantation fécale croisée de rats ou de souris d’humeurs différentes. Deux souches de souris qui possèdent des habitudes comportementales distinctes peuvent échanger celles-ci par transplantation de leur microbiote. Des souris timides et anxieuses qui réagissent fortement au stress, deviennent de véritables exploratrices, et vice-versa. Le microbiote est également mis en cause chez des enfants présentant des douleurs abdominales périodiques, ou encore dans l’autisme.
Un certain nombre de travaux relient le microbiote à l’apparition de maladies allergiques, auto-immunes ou inflammatoires à partir d’une théorie, la théorie hygiéniste, qui stipule que l’excès d’hygiène et d’antibiotiques a favorisé leur essor. Cette hypothèse hygiéniste est née d’observations montrant que dans les familles nombreuses, rhumes des foins et eczémas frappaient plus souvent les aînés, moins exposés que leurs cadets aux infections et au défaut d’hygiène. Ceci suggérait que l’exposition en bas âge aux microbes était nécessaire à l’éducation du système immunitaire. Cette idée fut confortée par le fait que les enfants de milieux ruraux, en contact avec une grande variété de microbes, sont souvent moins à risque de devenir asthmatiques et allergiques. Or les quatre ou cinq dernières décennies ont été marquées, dans les pays qui ont adopté des normes exigeantes d’hygiène, par une diminution considérable des maladies infectieuses telles que l’hépatite, la tuberculose, la rougeole ou le rhumatisme streptococcique. Simultanément, on a assisté à une augmentation spectaculaire des affections de nature allergique ou dysimmunitaire, telles que les maladies inflammatoires du colon – parmi lesquelles la maladie de Crohn –, le diabète insulino-dépendant de type 1 ou la sclérose en plaques. La fréquence de ces maladies suit un gradient décroissant en partant des pays du Nord vers ceux du Sud.
Agir contre les effets délétères du microbiote
Probiotiques, prébiotiques, xénobiotiques (substances produites par les bactéries), transplantations fécales sont autant de moyens pour modifier notre microbiote et ainsi potentiellement agir sur ces menaces.
ll existe plusieurs types de probiotiques qui se distiguent et se concurrencent par leurs bienfaits sur la santé, et plus spécialement leurs performances intestinales. Identifiées par genres, espèces, capacités d’adhésion, les bactéries et levures des probiotiques correspondent à plusieurs catégories de microbes. Les bacilles lactiques groupent aujourd’hui plus de cinquante espèces de lactobacilles. De multiples résultats démontrent que les probiotiques peuvent gagner l’intestin, survivre et se développer, même à titre transitoire, et accroître ainsi la diversité du microbiote. Mais il faut admettre que leur impact sur la santé est encore faible si on le compare à celui de l’alimentation ou des antibiotiques. La part de l’environnement, de la nourriture ou de la diète sur l’effet observé reste difficile à quantifier. Une des questions essentielles, celle qui résume toutes les autres, est de savoir déterminer si les probiotiques ont un impact sur la santé de l’homme et pas seulement sur l’écologie du microbiote. Cette preuve n’a pas encore été apportée, particulièrement au regard de la longue liste des maladies qu’une dysbiose du microbiote est supposée entraîner.
Les prébiotiques réduisent le nombre de pathogènes, une qualité attestée par l’incidence diminuée des diarrhées infectieuses et la moindre utilisation des antibiotiques. Il reste à en comprendre le mécanisme, qu’il s’agisse d’une redistribution de la colonisation des pathogènes par modification du biofilm, ou d’une stimulation des réponses innées et adaptatives du système immunitaire par les bactéries commensales.
Les xénobiotiques agissent sur la diversité de notre microbiote par l’action directe des antibiotiques sur la flore microbienne, qu’ils modifient ou détruisent selon les cas. Ici encore, la métagénomique permet d’appréhender ces effets, comme cela a été étudié pour certains antibiotiques de la famille des fluoroquinolones. On observe, trois à quatre jours après la prise du médicament, un effet important et rapide sur le microbiote intestinal, avec perte de diversité bactérienne et redistribution des communautés microbiennes. Qu’ils soient à large spectre ou non, les antibiotiques déséquilibrent notre flore, et à travers ce phénomène, ont un impact indirect sur de nombreuses maladies, notamment sur l’obésité. A cet égard, la perturbation de la flore intestinale par des antibiotiques pris dans les premières semaines de la vie est très certainement à éviter.
Les premières publications de l’utilisation de la transplantation fécale chez l’homme datent de 1958. Si ce traitement fécal a pour principale indication l’infection bactérienne à Clostridium difficile, les relations de plus en plus évidentes entre les anomalies du microbiote, la perte de sa biodiversité, le déséquilibre de ses fonctions et nombre de pathologies plaident en faveur de son utilisation dans d’autres maladies. L’avenir dira si le syndrome du colon irritable, les maladies inflammatoires de l’intestin, les allergies, l’obésité, l’autisme ou l’anorexie mentale, tout autant que le diabète de type 1 ou d’autres affections auto-immunes pourront bénéficier de cette modalité d’utilisation du microbiote humain, qui viendra alors s’ajouter à la panoplie des thérapeutiques déjà existantes.
Conclusions
L’étude du microbiote ouvre un nouveau paradigme en microbiologie, qui devrait intéresser toutes les sciences de la médecine et de la biologie, favoriser une approche pluridisciplinaire et associer la recherche académique et industrielle à son étude et à ses relations avec de nombreuses pathologies dites non transmissibles. C’est là un nouveau défi pour la recherche médicale reliant l’étude de l’écologie microbienne à une nouvelle approche environnementale, celle du corps humain.
[2] Debré P. Les révolutions de la biologie et le comportement humain, 2020, Odile Jacob Ed.

