Alain Delacroix
Professeur honoraire, chaire « Chimie industrielle – Génie des procédés » du Conservatoire national des arts et métiers
Il existe trois principaux éléments indispensables aux plantes : l’azote, le phosphore et le potassium (NPK Azote, Phosphore et Potassium). On trouve ces deux derniers dans la nature : le phosphore sous forme de phosphates dans des gisements naturels, en particulier au Maroc (on le traite par l’acide sulfurique pour le rendre soluble) et le potassium sous forme de sylvinite, que l’on trouve en Alsace. Quant à l’azote, bien qu’il soit le constituant principal de l’atmosphère, les plantes n’arrivent pas à l’assimiler car la molécule de diazote, où les deux atomes sont reliés par une triple liaison, est extrêmement stable. Seuls quelques plantes et les éclairs d’orages arrivent à la scinder. Depuis la nuit des temps, on utilise pour ce faire l’urine animale contenue dans les fumiers contenant de l’urée (NH2-CO-NH2). Ce procédé étant d’une efficacité médiocre, on a recours à l’ammoniac obtenu, entre autres, lors de la distillation de la houille. Avec le développement de l’agriculture intensive, les sources d’azote sont devenues insuffisantes et on a utilisé les gisements de guano et ceux de caliche du Chili, qui sont des nitrates impurs. A la fin du XIXe siècle, des milliers de grands bateaux à voile passaient le cap Horn pour récupérer ce précieux engrais.
Ce nitrate était devenu aussi la source d’acide nitrique en amont de tous les explosifs. Il remplaçait avantageusement le salpêtre, long à récupérer ou à fabriquer, avec de mauvais rendements. Par ailleurs, la poudre noire dont il était le constituant principal avait fait son temps.
Avant la guerre de 14-18, les Allemands, qui pressentaient que leur approvisionnement stratégique en nitrate serait bloqué par la marine anglaise, ont cherché et réussi à réaliser la synthèse de l’ammoniac à partir de l’azote de l’air et de l’hydrogène. Ce sont Haber et Bosch qui ont pu aboutir à cette extraordinaire synthèse industrielle en 1913. C’est une magnifique performance sur le plan chimique, physicochimique, thermodynamique et de génie chimique. Les conditions impliquaient alors des pressions de plusieurs centaines de bars nécessitant une structure et une métallurgie pour le réacteur très particulière. C’est, entre autres, avec ce procédé que les Allemands ont produit les millions de tonnes de trinitrotoluène, leur explosif de base lors de la première guerre mondiale (les Français utilisaient plutôt l’acide picrique : le trinitrophénol).
A Oppau, après la guerre, BASF possédait une usine d’ammoniac qu’elle avait modifiée pour fabriquer des engrais, dont le nitrate d’ammonium mélangé à du sulfate d’ammonium. Ce mélange étant plus ou moins hygroscopique, il se compactait et les ouvriers utilisaient un explosif pour fragmenter cette énorme masse de 4000 tonnes. Cette opération fut réalisée des milliers de fois jusqu’au 21 septembre 1921 où une énorme explosion se produisit. On dénombra alors plus de 500 morts, 2000 blessés, et la ville fut pratiquement détruite. La cause réelle de l’explosion ne semble pas avoir été découverte. On en a déduit toutefois qu’il fallait éviter de tirer à l’explosif dans des tas de nitrate d’ammonium !
En avril 1947, le Liberty ship français Grandcamp est en cours de chargement à Texas City et contient plus de 2000 tonnes de sacs de nitrate d’ammonium et divers produits combustibles, dont des balles de ficelle de sisal. Ce nitrate d’ammonium provient de surplus de guerre et est peut-être impur. Il prend feu vers 8 h du matin. Le capitaine, logiquement, ferme tous les panneaux et envoie de la vapeur dans la cale. Malheureusement, le nitrate d’ammonium contient beaucoup d’oxygène et peut brûler en atmosphère confinée. A 8h30 on évacue le navire et on tente de le remorquer au loin mais à 9h12 le bateau explose. L’explosion provoque un gigantesque incendie du site industriel et continue par la combustion du cargo High Flyer, qui contient 1000 tonnes de soufre et près de 1000 tonnes de nitrate d’ammonium. Il explose à son tour le lendemain et met le feu à un stock de nitrate d’ammonium, qui brûle sans exploser. On déplore plus de 500 morts et près de 3000 blessés. C’est une des premières catastrophes à effet domino, qui servira d’exemple pour éviter les accidents industriels en chaîne.
Le 23 juillet 1947, un autre Liberty ship, l’Ocean Liberty, accoste à Brest avec à son bord 3300 tonnes de nitrate d’ammonium et de nombreux produits combustibles, dont de la peinture et de la paraffine. Vers 12h30, de la fumée sort de la cale qui contient le nitrate. Comme on est au courant de la catastrophe de Texas City, on tente de remorquer le bateau hors du port. Malheureusement, il s’échoue sur un banc de sable. On tente alors de le saborder mais à 17h24, le cargo explose. Des débris du navire et de sa cargaison en flamme mettent le feu à la ville, déjà bien frappée par la guerre. On déplore 26 morts et près de 500 blessés. Plus de 4000 maisons sont détruites.
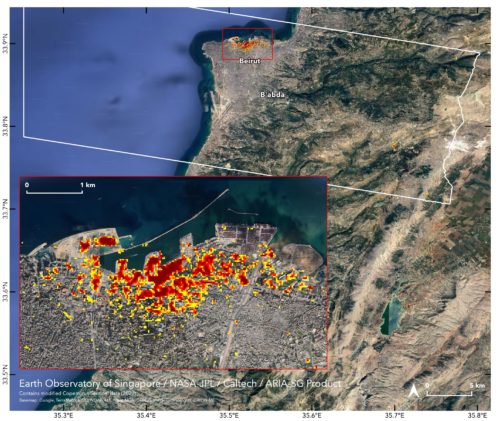
De ces deux dernières catastrophes, on a déduit qu’il ne fallait pas stocker du nitrate d’ammonium en milieu confiné avec des matières combustibles, règle qui a été respectée. Et pourtant, quatre-vingts ans jour pour jour après Oppau, l’usine AZF de Toulouse a explosé, et, probablement pour une raison encore différente, on vient de déplorer la catastrophe de Beyrouth.

