Alain Delacroix
Ancien professeur titulaire de la chaire « Chimie industrielle – Génie des procédés » du Conservatoire national des arts et métiers
Une explosion est le résultat d’une réaction physicochimique dont la vitesse est très élevée et qui génère une importante quantité d’énergie dans un temps très court. La brusque montée de pression correspondante crée une onde de choc dont la vitesse est un indicateur de sa puissance de destruction. Si cette vitesse est inférieure à la vitesse du son, c’est une déflagration, si elle est supérieure, c’est une détonation et dans ce cas, les effets brisants sont très importants. Les explosifs militaires ont une vitesse de détonation qui peut être supérieure à 9000 m/s. Un explosif est alors une molécule ou un ensemble de molécules qui libèrent une grande quantité de gaz en un temps très court.
De très nombreux produits peuvent exploser. On distingue ceux qui sont occasionnels, tel le nitrate d’ammonium, et ceux qui sont intentionnels, les explosifs civils (mines, travaux publics) et militaires. Il existe des dizaines de groupes explosophores dont la présence dans une molécule peut conduire à la rendre explosive, par exemple NO2, -O-O-, etc. Des méthodes existent permettant de prévoir et de calculer la dangerosité d’une molécule.
La poudre noire était connue des Chinois depuis le début de l’ère chrétienne mais c’est au XIVe siècle que commence son utilisation balistique. C’est un mélange de nitrate de potassium KNO3, de soufre et de carbone. En réagissant, ce mélange fournit une grande quantité de gaz selon la réaction :
2 KNO3 + S + C -> K2S + 3CO2 + N2
En dehors du soufre et du charbon trouvés à l’état naturel, le nitrate, appelé salpêtre, était recherché jusqu’au XVIIIe siècle au fond des étables puisqu’il constitue les efflorescences caractéristiques sur les pierres calcaires humides. Le mélange, difficile à réaliser, était obtenu par un broyage très fin dans des moulins situés dans les poudreries. Ceux-ci explosaient souvent et le poudrier devait marcher avec des chaussons de cuir et sans cogner le sol. C’était le célèbre pas du poudrier ! (le pétardier, qui faisait sauter les portes des forteresses au XVIe siècle, avait, lui aussi, une durée de vie fort limitée). En 1794, un stock de 1000 tonnes de poudre a explosé au château de Grenelle faisant des centaines de morts. On en a déduit à l’époque qu’il fallait éloigner les poudreries des villes. La poudrerie de Grenelle est alors transférée à Meudon !
Compte tenu de l’instabilité de la poudre noire, les chimistes ont commencé, dès le XVIIIe siècle, à chercher des produits plus sûrs. Berthollet, avec du sucre et du chlorate de potassium, a inventé les cheddites. En 1846, Bottger et Schonbein fabriquent la nitrocellulose (coton poudre), stabilisée plus tard par Paul Vieille. La même année, Sobrero découvre les propriétés du nitrate de glycérol, d’où la nitroglycérine stabilisée par Alfred Nobel, ce qui a conduit à la dynamite.
A la fin du XIXe siècle et pendant la guerre de 14-18, compte tenu des quantités énormes impliquées, on a développé une industrie chimique lourde. En France, on a utilisé l’acide picrique et en Allemagne, le trinitrotoluène (TNT). Ces deux produits ont les formules simples suivantes :
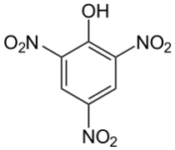
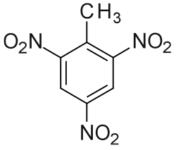
Entre les deux guerres, on a découvert l’hexogène et la pentrite, produits qui commencent à avoir des formules sophistiquées et sont difficiles à fabriquer. L’hexogène a une vitesse de détonation de 8700 m/s. Un explosif moderne est maintenant l’association de groupes oxydants tels que NO2 avec un squelette carboné instable associé à une structure solide complexe.
Cependant, de très nombreuses molécules ou mélanges peuvent exploser et sont faciles à produire. Il suffit souvent de mélanger un produit très oxydant : nitrate, perchlorate, eau oxygénée, avec un produit réducteur : soufre, sucre, hydrocarbure, acétone, etc. Un explosif bien connu est un mélange de fioul et de nitrate d’ammonium.
Quant au TATP, de sinistre réputation, c’est un peroxyde, le triacétone triperoxyde, découvert en 1895 par Richard Wolffenstein. Il se prépare à partie d’acétone et d’eau oxygénée en milieu acide. C’est un solide blanc dont la vitesse de détonation est de l’ordre de 5000 m/s. Ses matières premières étant très accessibles et sa préparation étant relativement facile par un chimiste, il est maintenant souvent utilisé par les terroristes. Sa formule développée sous la forme trimère est la suivante :
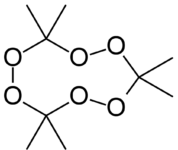
Il existe donc de très nombreuses molécules ou mélanges de produits susceptibles de conduire à des explosions occasionnelles ou intentionnelles. Même un kilogramme de farine pulvérisé dans l’air et enflammé peut donner une forte déflagration. Des personnes mal intentionnées et pas forcément bonnes chimistes disposent donc malheureusement d’un large éventail de méthodes et produits pour perpétrer leurs forfaits.