Jeanne Brugère-Picoux
Professeur honoraire de pathologie médicale du bétail et des animaux de basse-cour (Ecole nationale vétérinaire d’Alfort), membre de l’Académie nationale de médecine, présidente honoraire de l’Académie vétérinaire de France

Un article paru dans The Lancet le 10 août 2022 rapporte l’observation en France d’un premier cas mondial de transmission du virus de la variole du singe de l’Homme au chien [1]. Le chien contaminé appartenait à deux hommes ayant consulté à l’hôpital de la Pitié-Salpêtrière le 10 juin et présentant les lésions classiques de la maladie signalées depuis début mai dans leur communauté homosexuelle : asthénie, céphalées, hyperthermie, ulcérations anales et, chez l’un d’eux, éruption vésiculo-pustuleuse sur le visage, les oreilles et les jambes. L’infection virale a été confirmée par PCR sur les prélèvements réalisés chez les deux patients (peau et oropharynx pour l’un, anus et oropharynx pour l’autre). Douze jours après l’apparition de ces symptômes, leur chien lévrier mâle âgé de quatre ans, sans antécédent de maladie, a présenté des lésions cutanéo-muqueuses (pustules sur l’abdomen et fine ulcération anale). Par PCR, le virus de la variole du chien a été identifié sur divers prélèvements (pustules cutanées, anus, cavité buccale). Il était identique à celui des propriétaires (et au clade hMPXV-1, lignée B.1 répandu depuis avril 2022 dans les régions non endémiques). Les propriétaires ont signalé qu’ils dormaient avec le chien dans leur chambre tout en ayant évité tout contact de ce chien avec d’autres animaux ou des personnes dès l’apparition de leurs premiers symptômes (soit 13 jours avant les troubles cutanés chez le chien).
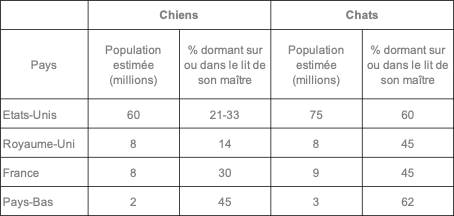
Le risque lié à la présence d’un chien ou d’un chat dans la chambre de son maître n’est pas nouveau. Il peut même paraître surprenant de constater le nombre de personnes acceptant de laisser leur animal dormir dans leur lit. Une enquête publiée en 2011 et réalisée de 1974 à 2010 aux Etats-Unis, aux Pays-Bas, en France et au Royaume-Uni a permis de noter que 14 à 62% des propriétaires dorment avec leur chat ou leur chien (cf. tableau). On oublie combien cette habitude peut favoriser la transmission de diverses maladies (bartonellose ou maladie des griffes du chat ; Capnocytophaga canimorsus, bactérie présente dans la salive du chien et pouvant provoquer une septicémie mortelle ; pasteurellose ; staphylococcies ; parasitoses) [2]. Dans le cas de la Covid-19, une enquête canadienne a montré que le temps passé avec un contact entre le chien et son maître n’avait pas joué un rôle dans la contamination de l’animal mais qu’il n’en était pas de même pour les chats qui étaient plus à risque d’être contaminés s’ils dormaient dans le lit de leur maître [3].
Dans cette enquête, les poxvirus n’étaient pas cités. Alors que la variole a été la première maladie pouvant être prévenue par la vaccination et ainsi la première à être éradiquée, les autres infections à poxvirus ont souvent été sous-estimées alors que certaines sont zoonotiques. En premier lieu, il faut souligner que ces poxviroses zoonotiques sont souvent bénignes, sauf chez les personnes immunodéprimées. C’est pourquoi l’infection humaine reste une zoonose sous-estimée car peu fréquente et de ce fait rarement reconnue immédiatement par le clinicien (cela a pu être aussi le cas pour la variole du singe, qui a pu ainsi se propager pendant un certain temps sans être détectée avant mai 2022 en dehors de l’Afrique du fait de son mode particulier de propagation par des relations sexuelles dans la communauté homosexuelle masculine). Les poxvirus les plus souvent rencontrés chez l’Homme sont le cowpox (orthopoxvirus) et l’ecthyma contagieux (parapoxvirus), très connu chez les petits ruminants mais beaucoup moins des particuliers propriétaires de moutons ou de chèvres «tondeuses». Dans le cas du cowpox, des cas graves exceptionnels ont cependant pu être observés. Bien que l’infection par le cowpox soit sporadique, le virus est endémique en Europe du Nord, avec une augmentation du nombre de cas depuis une vingtaine d’années, peut-être du fait de l’arrêt de la vaccination contre la variole [4]. Le réservoir de ce poxvirus est constitué par des petits rongeurs sauvages, notamment le rat d’égout ou surmulot (Rattus norvegicus), espèce dont dérive le rat domestique d’élevage, facile à apprivoiser comme rat de laboratoire ou nouvel animal de compagnie (NAC). C’est ainsi qu’en Europe nous avons connu en 2009 une épidémie humaine avec des rats importés de Hongrie en tant que NAC [5]. Le rat peut infecter l’Homme et de nombreuses espèces animales, le plus souvent par morsure (chiens, chats, bovins, chevaux, singes, lamas, éléphants…). Si les cas sont rares chez le chien (infecté par morsure de la truffe), ils sont plus fréquents chez le chat du fait de son comportement de chasseur (le premier cas félin de cowpox a été décrit en 1978). Ce contact étroit du chat avec les rongeurs explique qu’il soit la source la plus importante des infections humaines.
Dans le cas de l’orthopoxvirus de la variole du singe, en dehors des singes utilisés dans des laboratoires à partir desquels le virus fut isolé pour la première fois en 1958 (d’où la dénomination de ce virus), on ne connaît pas l’espèce hôte réservoir de ce virus. On a souvent considéré en République démocratique du Congo (RDC), où la maladie est endémique, que l’infection humaine résultait d’un contact avec un animal sylvestre infecté, bien que l’espèce hôte réservoir soit actuellement inconnue. Diverses espèces sont suspectées, qu’il s’agisse d’animaux sauvages devenus familiers ou chassés pour leur consommation (viande de brousse) : le Cricetomys gambianus (rat de Gambie), le Cercopithecus ascanius (singe à queue rousse) et les écureuils africains, en particulier les genres Funisciurus et Heliosciurus rufobrachium (écureuil soleil à pattes rouges) [6,7]. Le seul MPXV isolé d’un mammifère sauvage a été obtenu à partir d’un écureuil à cordes moribond (Funisciurus anerythrus) collecté lors d’une enquête sur une épidémie en RDC [8,9].
L’exemple de l’épidémie de variole du singe observée en mai 2003 dans le Midwest américain est significatif pour plusieurs raisons :
- elle a confirmé l’origine zoonotique suspectée en Afrique de cette poxvirose par l’importation du Ghana de rats de Gambie (ou cricétomes des savanes) [10], ces rats africains d’origine sauvage apparemment sains étant vendus comme nouveaux animaux de compagnie (NAC) ;
- ces rats de Gambie ont joué le rôle de réservoir asymptomatique comme dans le cowpox avec le rat d’égout (ou de compagnie) en contaminant dans l’animalerie des chiens de prairie (Cynomys ludovicianus), autres rongeurs NAC autochtones de la famille des Sciuridae ;
- les chiens de prairie furent malades mais aussi les vecteurs secondaires d’une contamination humaine avec 71 cas, dont plusieurs enfants ;
- les huit premiers cas humains n’ont pas été reconnus (comme ce fut le cas pour les premiers patients atteints par la nouvelle épidémie de variole du singe qui présentaient des lésions génitales) et il a fallu plus d’une semaine pour que ces cas soient signalés aux autorités de santé publique [11] ;
- ce fut la seule importante épidémie de variole simienne observée dans un pays non africain et due à des animaux de compagnie.
La contamination d’un chien par ses propriétaires faisant partie de la communauté homosexuelle, contaminée dans plus de 95% des cas observés depuis mai 2022* dans la pandémie actuelle, ajoute une nouvelle espèce sensible au MPXV. Cet agent pathogène réémergent ne se limite plus aux régions endémiques africaines et présente le risque mondial d’occuper la niche écologique laissée vacante par la variole. Le problème sera de savoir si le MPXV s’établira plus dans un réservoir animal que dans la population humaine s’il continue à se propager.
Connaissant le grand nombre d’espèces animales sensibles à un autre orthopoxvirus zoonotique (cowpox), on ne peut exclure dans ce cas la possibilité d’autres espèces sensibles au MPXV, en particulier parmi les animaux de compagnie, et le risque de rongeurs porteurs asymptomatiques. C’est pourquoi nous soulignerons à nouveau la recommandation de l’Académie nationale de médecine, dans son communiqué du 8 juillet 2022, «d’éviter le contact entre les cas et les animaux pendant la maladie jusqu’à la chute des croûtes» [13]. Une épidémiosurveillance concernant le risque d’une contamination zoonotique par le MPXV de l’Homme vers l’animal ou de l’animal vers l’Homme et l’application stricte des mesures de biosécurité préconisées pendant la période d’isolement de 21 jours dans les cas humains s’avère nécessaire.
En conclusion, nous ne pouvons que reprendre celle de notre confrère Alexis Lécu, responsable du zoo de Vincennes, à propos du Sars-CoV-2 [14] : «Les tribulations de ce virus chez l’animal nous enseignent finalement la même leçon que son apparition en 2019 : nous devons rapidement remettre de la distance avec l’animal, pour notre bien à tous».
[1] Seang S, Burrel S, Todesco E, Leducq V, Monsel G, Le Pluart D, et al. Evidence of human-to-dog transmission of monkeypox virus. The Lancet. août 2022;S0140673622014878.
[2] Chomel BB, Sun B. Zoonoses in the Bedroom. Emerg Infect Dis. févr 2011;17(2):167‑72.
[3] Bienzle D. Cats may catch Covid-19 from sleeping on their owner’s bed. EurekAlert. European Congress of Clinical Microbiology & Infectious Diseases (ECCMID, 30-Jun-2021); 2021.
[4] Rosone F, Sala MG, Cardeti G, Rombolà P, Cittadini M, Carnio A, et al. Sero-Epidemiological Survey of Orthopoxvirus in Stray Cats and in Different Domestic, Wild and Exotic Animal Species of Central Italy. Viruses. 19 oct 2021;13(10):2105.
[5] Campe H, Zimmermann P, Glos K, Bayer M, Bergemann H, Dreweck C, et al. Cowpox Virus Transmission from Pet Rats to Humans, Germany. Emerg Infect Dis. mai 2009;15(5):777‑80.
[6] Walker M. Monkeypox Virus Hosts and Transmission Routes: A Systematic Review of a Zoonotic Pathogen. Biological Sciences Undergraduate Honors Theses [Internet]. 1 mai 2022; Disponible sur: https://scholarworks.uark.edu/biscuht/69
[7] Monroe BP, Doty JB, Moses C, Ibata S, Reynolds M, Carroll D. Collection and Utilization of Animal Carcasses Associated with zoonotic Disease in Tshuapa District, the Democratic Republic of the Congo, 2012. Journal of Wildlife Diseases. juill 2015;51(3):734‑8.
[8] Reynolds MG, Carroll DS, Olson VA et al. C. A Silent Enzootic of an Orthopoxvirus in Ghana, West Africa: Evidence for Multi-Species Involvement in the Absence of Widespread Human Disease. The American Journal of Tropical Medicine and Hygiene. 1 avr 2010;82(4):746‑54.
[9] Jezek Z, Grab B, Szczeniowski MV, Paluku KM, Mutombo M. Human monkeypox: secondary attack rates. Bull World Health Organ. 1988;66(4):465‑70.
[10] Centers for Disease Control and Prevention (CDC). Update: multistate outbreak of monkeypox–Illinois, Indiana, Kansas, Missouri, Ohio, and Wisconsin, 2003. MMWR Morb Mortal Wkly Rep. 11 juill 2003;52(27):642‑6.
[11] Reed KD, Melski JW, Graham MB, Regnery RL, Sotir MJ, Wegner MV, et al. The Detection of Monkeypox in Humans in the Western Hemisphere. N Engl J Med. 22 janv 2004;350(4):342‑50.
[12] CDC. 2022 Monkeypox Outbreak Global Map [Internet]. 2022 [cité 16 août 2022]. Disponible sur: https://www.cdc.gov/poxvirus/monkeypox/response/2022/world-map.html.
[13] Académie nationale de médecine. Variole du singe: zoonose et infection sexuellement transmissible (IST) [Internet]. Communiqué; 2022. Disponible sur: https://www.academie-medecine.fr/variole-du-singe-zoonose-et-infection-sexuellement-transmissible-ist/.
[14] Lécu A. Covid : retour sur 30 mois de tribulations d’un virus humain chez l’animal [Internet]. The Conversation. [cité 27 juill 2022]. Disponible sur: http://theconversation.com/covid-retour-sur-30-mois-de-tribulations-dun-virus-humain-chez-lanimal-187552

